Giấy chứng nhận phù hợp chuyên luận dược điển châu Âu CEP (Certification of suitability to the monographs of the European Pharmacopoeia) dùng để xác nhận tiêu chuẩn của dược chất hoặc nguyên liệu làm thuốc tuân thủ với các quy tắc được nêu trong chuyên luận của Dược điển Châu Âu (EP).

Cơ quan cấp giấy chứng nhận CEP là Hội đồng Châu Âu về Chất lượng thuốc (EDQM).
Nhà sản xuất, nhà cung cấp hoặc đại diện hợp pháp của dược chất hoặc nguyên liệu làm thuốc sẽ tiến hành các thủ tục theo quy định của EDQM để xin cấp giấy chứng nhận CEP cho hoạt chất hoặc nguyên liệu làm thuốc và là chủ sở hữu của giấy chứng nhận CEP này.
Link tra cứu giấy chứng nhận CEP: https://extranet.edqm.eu/publications/recherches_CEP.shtml
Cách tra cứu: Nhập tên hoạt chất/nguyên liệu vào ô tìm kiếm và chọn “Search”, kết quả sẽ trả về theo tên hoạt chất, chủ sở hữu giấy chứng nhận CEP, số giấy chứng nhận, ngày cấp, tình trạng của giấy chứng nhận.
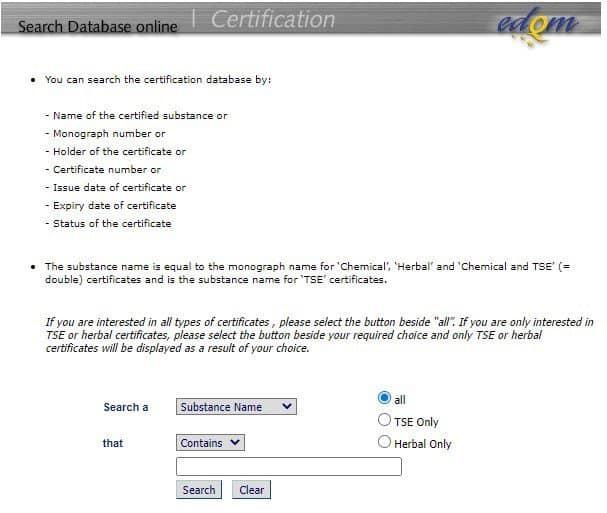
Hướng dẫn cách đọc hiểu thông tin trên giấy chứng nhận CEP: (Xem hình ảnh minh họa đính kèm bài viết)
Lưu ý khi nộp giấy chứng nhận CEP trong hồ sơ đăng ký thuốc:
– Giấy chứng nhận CEP cần phải được hợp pháp hóa lãnh sự
– Cần có thông tin về việc chủ sỡ hữu giấy chứng nhận ủy quyền cho công ty đăng ký sử dụng CEP trong hồ sơ đăng ký thuốc thành phẩm tại phần Declaration of Access (DoA)
Theo quy định tại điểm c, khoản 5, điều 24, thông tư 08/2022/TT-BYT, trường hợp trong hồ sơ đăng ký thuốc có nộp CEP của dược chất, phần hồ sơ dược chất có thể được thay thế bằng:
– Giấy chứng nhận tuân thủ dược điển châu Âu (CEP) đối với dược chất kèm theo tất cả các phụ lục được ban hành bởi Hội đồng châu Âu về chất lượng thuốc (EDQM);
– Số liệu phân tích lô dược chất;
– Nếu thời hạn phải kiểm tra lại chất lượng dược chất không nêu trong CEP, nộp số liệu nghiên cứu độ ổn định của dược chất.











